El Study Tracking System – STS (Sistema de seguimiento de estudios) está diseñado para compañías que necesitan gestionar reportes y registro de información de visitas de monitoreo en estudios clínicos, de acuerdo con los requerimientos de la industria, como las CROs (Organizaciones de Investigación por Contrato).
El STS es un sistema basado en la web que permite la creación, revisión y aprobación de los reportes de las visitas de monitoreo durante la conducción de un estudio clínico. El sistema incluye la programación de las visitas y el acceso a la base de datos del estudio, donde se registran elementos de acción, desviaciones del protocolo, información de seguridad, registros SDV, etc. Así mismo, se pueden consultar los plazos de presentación/aprobación de los informes de las visitas de seguimiento y los reportes obtenidos para hacer un monitoreo detallado del estado del estudio. Esta información también puede ser analizada a través de tableros de control personalizados, que permiten visualizar los indicadores y métricas del estudio en tiempo real para la toma de decisiones oportuna.

Multiestudio
y multisitio

Reportes en formato estructurado, con opción de sugerir correcciones, comentarios y aprobar

Descargar reportes en formato PDF

Agendar y completar formatos de acuerdo al protocolo directamente en el sistema

Garantiza el registro completo de los datos con campos obligatorios

Asignar proyectos a diferentes usuarios con el rol de administrador

Función para auditorías y validación de procesos

Importación masiva de datos desde Excel

En el STS, los CRAs (Clinical Research Associates) completan los reportes de monitoreo sin perder información, pues la información se guarda en tiempo real; así mismo, pueden planear sus actividades de seguimiento y consultar la información del estudio y el centro de investigación utilizando la base de datos.
Los Proyect Managers – PM (gerentes de proyecto) pueden manejar múltiples centros, revisar informes y administrar información del estudio; personal específico puede acceder a la información para apoyar la planificación y las actividades de seguimiento (p. ej., CTA) y realizar actividades de supervisión (p. ej., gerentes de línea, área de calidad). Dentro del STS, los monitores y gerentes de proyectos certifican que todos los procesos se llevan a cabo de acuerdo con las mejores prácticas mediante la firma electrónica de tareas.
De acuerdo a los requisitos del estudio se pueden generar:
Este módulo permite crear y configurar visitas en el sistema y establecer un Clinical Research Associate – CRA (Asociado de investigación) a cargo, incluyendo:
Crear
Visita
Auditoría
de Visita
Los tableros de reportes brindan acceso a resúmenes sobre el estado de cada visita (creada, pendiente de aprobación o aprobada).
Creación de reportes:
En esta sección el CRA recolecta la información durante la visita y puede complementar el reporte con más información posteriormente. Este módulo permite personalizar secciones como centro en entrenamiento, muestras del estudio, locaciones y equipo, eventos adversos serios (SAE), comentarios generales, consentimientos informados y acciones.
Por ejemplo, en la sección Acciones, los CRA pueden registrar desviaciones del protocolo, crear items problema, asignar fechas abiertas o cierres, determinar acciones requeridas y agregar notas.
Crear
Reporte
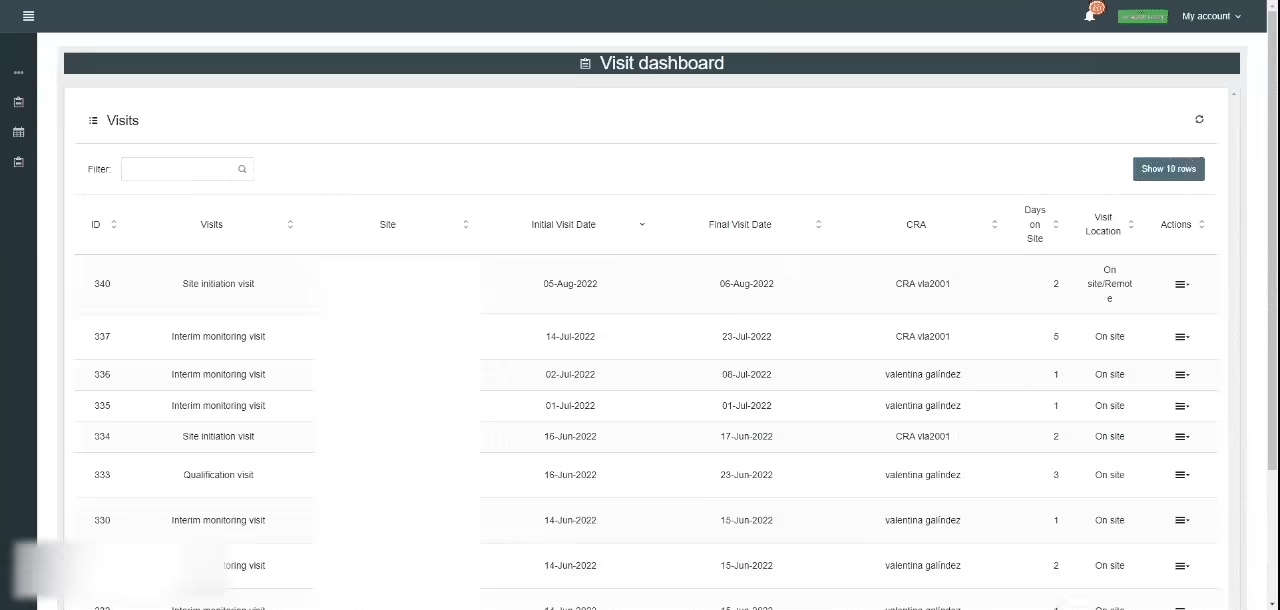
Tablero
de Reportes
Base
de Datos
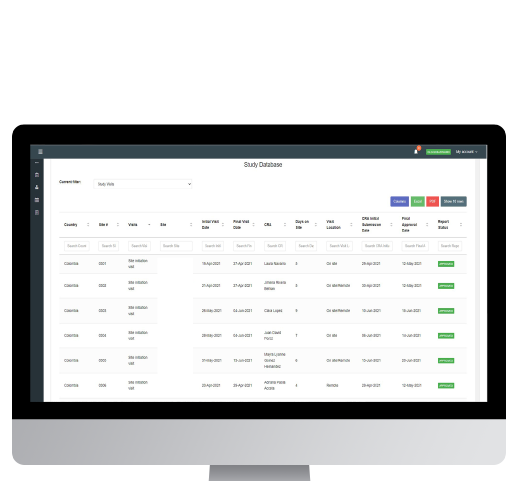
El módulo de base de datos del estudio permite acceder a toda la información de las visitas de los estudios, incluyendo detalles claves como país, centro de investigación, tipo de visita, CRA a cargo, estado, etc. Estos reportes pueden ser descargados en formato Excel o en formato PDF.
Acceda a paneles de control con métricas personalizadas por estudio y obtenga una vista general de indicadores como informes de eventos adversos serios (SAE), tiempos de SAE, tipos de informes y fechas de registro de notificaciones de patrocinadores, en una forma gráfica.
Esta funcionalidad es una herramienta que hace más eficientes a las CRO, y les permite enfocarse en el análisis de los datos y la rigurosidad de las actividades de monitoreo.
Accesible para patrocinadores, CROs y centros de investigación pequeños y medianos
Información en tiempo real para la toma de decisiones basada en datos
Estudios con inicios rápidos
Soluciones interoperables entre sí e integrables con soluciones de terceros
Soluciones validadas en buenas practicas clínicas y en cumplimiento de normativa internacional
Arquitectura escalable on-off a demanda
Experiencia en países de bajos y medianos ingresos
Funcionalidades especiales para estudios de vacunas
¡Agenda una reunión con nosotros en un clic!

Integra IT.
En Integra IT, utilizamos la innovación en tecnología para la recopilación, el acceso y la vigilancia de datos en ensayos de ciencias de la vida en todas las fases de manera eficiente. Ofrecemos un portafolio completo de soluciones 100% en la nube de acuerdo con las regulaciones GCP y FDA 21 CFR Parte 11, con el objetivo de hacer que el trabajo de nuestros socios sea más fácil y efectivo. Desarrollamos soluciones dedicadas para empresas farmacéuticas, CRO y sitios.
Para Centros de Investigación.
Otras
Soluciones.
Para
CROs.
Quiénes Somos.