
6 Capacidades de los servicios de eCRF y de gestión de datos de Integra IT
Los datos son el activo más valioso de un ensayo clínico. Garantizar la calidad y precisión de los datos determina la obtención de las pruebas
Intega IT, Socio de Viedoc para América Latina y Mercados Emergentes
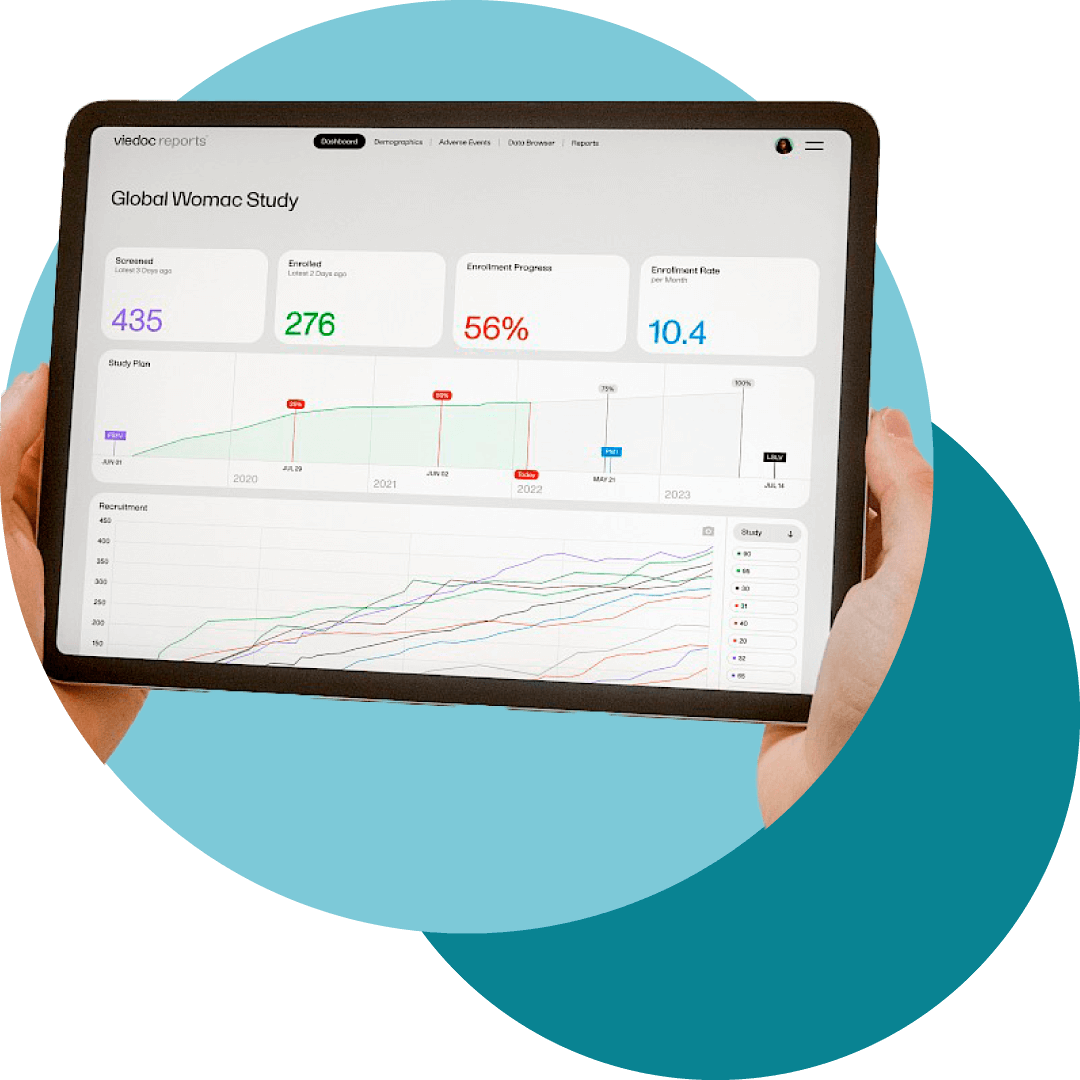

Intega IT, Socio de Viedoc para América Latina y Mercados Emergentes

Este paquete proporciona un electronic Case Report Form (eCRF) y una solución web, rentable y fácil de usar. Junto con nuestras soluciones móviles TriaPal ePRO y eCOA, mejoramos la gestión de datos clínicos a través de entregables superiores, ejecución oportuna y calidad excepcional.
Nuestro enfoque enfatiza la alta eficiencia, garantizando la transparencia, la integridad y la calidad de los datos durante todo el proceso del ensayo clínico.

Para saber más acerca de Viedoc
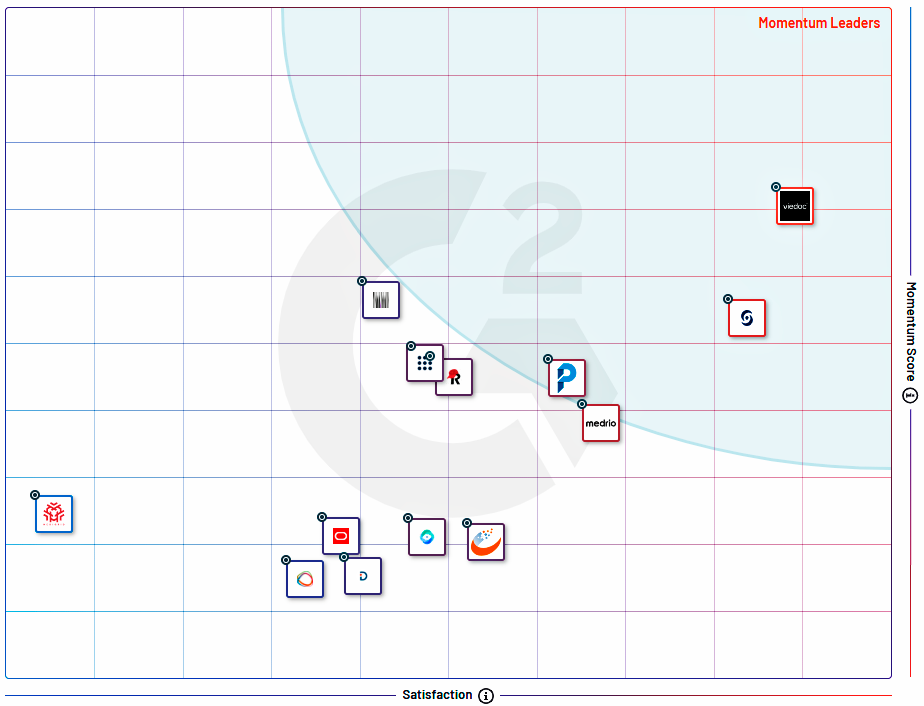
Accesible para patrocinadores, CROs y centros de investigación pequeños y medianos
Información en tiempo real para la toma de decisiones basada en datos
Estudios con inicios rápidos
Soluciones interoperables entre sí e integrables con soluciones de terceros
Soluciones validadas en buenas practicas clínicas y en cumplimiento de normativa internacional
Arquitectura escalable on-off a demanda
Experiencia en países de bajos y medianos ingresos
Funcionalidades especiales para estudios de vacunas

Los datos son el activo más valioso de un ensayo clínico. Garantizar la calidad y precisión de los datos determina la obtención de las pruebas

¡Los datos nos mueven! Nuestra solución y servicios de para captura electrónica de datos (EDC), Integra IT eCRF & Data Management Services aporta a los